PhysProf - Bohrsches Atommodell - Schalen - Animation - Elektronen

Fachthema: Bohrsches Atommodell
PhysProf - Ein Programm zur Visualisierung von Sachverhalten aus verschiedenen Teilgebieten der Physik mittels Simulationen und 2D-Animationen für die Schule, das Abitur, das Studium sowie für Lehrer, Ingenieure und alle die sich hierfür interessieren.
Online-Hilfe für das Modul
zur einfachen Darstellung der Belegung der Elektronenbahnen bekannter Elemente.
Dieses Unterprogramm ermöglicht die Durchführung der Steuerung entsprechender Abläufe zur Echtzeit und bietet die Möglichkeit, die Einflüsse relevanter Größen interaktiv zu untersuchen.
Es unterstützt dabei ein tiefergehendes Verständnis zu diesem Themengebiet zu erlangen und kann zum Lösen vieler diesbezüglich relevanter Aufgaben eingesetzt werden.

Weitere relevante Seiten zu diesem Programm

Themen und Stichworte zu diesem Modul:Bohrsches Modell - Bohr - Niels Bohr - Atommodell - Bohrsches Atommodell - Bohrsches Postulat - Bohrsche Postulate - Atome - Atomaufbau - Atombau - Atomar - Elemente - Chemische Elemente - Elektronen - Elektronenbahn - Elektronenbahnen - Energie - Atomkern- Atomkerne - Schalenmodell - Ordnungszahl - Elektronenschale - Elektronenschalen - Außenelektronen - Valenzelektron - Valenzelektronen - Name - Namen - Erklärung - Einfach erklärt - Einführung - Was - Wie - Weshalb - Was ist - Warum - Bedeutung - Was bedeutet - Arbeitsblatt - Arbeitsblätter - Unterrichtsmaterial - Unterrichtsmaterialien - Lernen - Grundlagen - Beschreibung - Beschriftung - Definition - Begriff - Begriffe - Aufgaben - Abituraufgaben - Abiturvorbereitung - Abitur - Abi - Leistungskurs - LK - Klassenarbeit - Klassenarbeiten - Anwendungsaufgaben - Postulat - Postulate - Schale - Schalen - Erste Schale - Zweite Schale - Dritte Schale - Vierte Schale - 1. Schale - 2. Schale - 3. Schale - 4. Schale - K-Schale - L-Schale - M-Schale - N-Schale - O-Schale - P-Schale - Q-Schale |
 |  |
Bohrsches Atommodell
Modul Bohrsches Atommodell
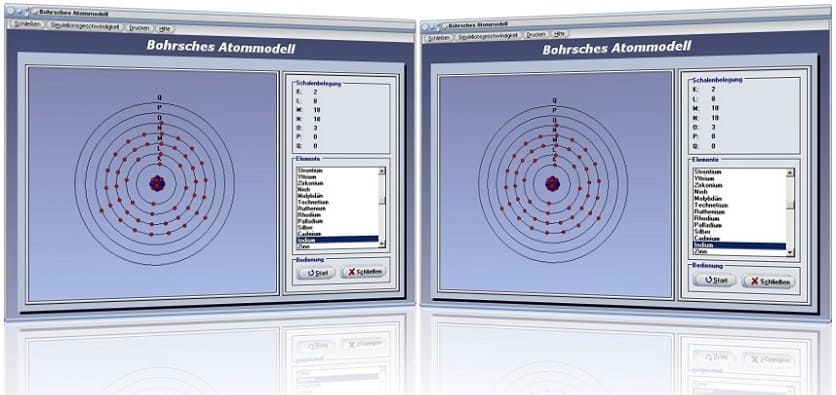
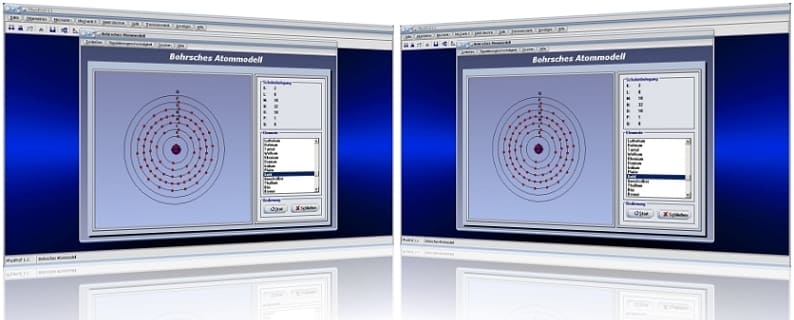
Mit Hilfe des Unterprogramms [Sonstiges] - [Bohrsches Atommodell] lassen sich die Belegungen der Elektronenbahnen aller bislang bekannter Elemente darstellen.

Bohrsches Atommodell - Abbildung 1

Bohrsches Atommodell - Abbildung 2
Im Jahre 1913 gelang es dem dänischen Physiker Niels Bohr mit einer Erweiterung des Rutherfordschen Atommodells das Wasserstoffspektrum zu erklären. In diesem Modell umkreist das negativ geladene Elektron aufgrund der Coulombschen Anziehungskräfte den positiv geladenen Atomkern. Er formulierte die nach ihm benannten Postulate (Bohrsche Postulate):
- Elektronen können einen Atomkern nur auf bestimmten Bahnen (Energieniveaus) umlaufen. Diese Bahnen sind konzentrisch um den Kern des Atoms angeordnet.
- Ein Elektron verfügt über eine bestimmte Energie. Wenn dieses auf eine sich weiter aussen liegende Bahn bewegt werden soll, so muss ihm Energie zugeführt werden und die Energie die ihm zugeführt wird darf keine Werte besitzen, welches dieses an einen Ort zwischen den Bahnen positionieren würde.
Postulat:
Als Postulat wird eine Aussage bezeichnet, die nicht bewiesen werden kann und dennoch nicht unbedingt falsch sein muss. Es handelt sich somit um eine unbeweisbare Aussage.
Nach der klassischen Elektrodynamik müsste ein Elektron, welches um den Atomkern kreist und somit eine Zentripetalbeschleunigung erfährt, als beschleunigte Ladung kontinuierlich elektromagnetische Wellen abgeben und daher aufgrund des Energieverlusts nach kurzer Zeit in den Kern stürzen. Im Gegensatz dazu gibt ein Elektron nach der Bohrschen Modellvorstellung keine Energie ab, solange es sich auf der entsprechenden Bahn befindet. Ein Elektron, welches sich nicht auf der innersten Schale befindet, kann spontan in einen tieferen Zustand übergehen und dabei Energie in Form eines Lichtquants (Photons) abgeben. In diesem Modul werden entsprechend diesen Vorstellungen die Elektronenbahnen dargestellt.
Programmbedienung
Wählen Sie aus der Liste ein entsprechendes Element aus und bedienen Sie die Schaltfläche Start, so wird die Bewegung der Elektronen auf ihren Schalen um den Atomkern simuliert.
Nachfolgend aufgeführt ist eine Tabelle der Elemente für welche die Schalenbelegung ausgegeben werden kann sowie derer Symbol-Kürzel.
| Element | Symbol | |
| 1 | Wasserstoff | H |
| 2 | Helium | He |
| 3 | Lithium | Li |
| 4 | Beryllium | Be |
| 5 | Bor | B |
| 6 | Kohlenstoff | C |
| 7 | Stickstoff | N |
| 8 | Sauerstoff | O |
| 9 | Fluor | F |
| 10 | Neon | Ne |
| 11 | Natrium | Na |
| 12 | Magnesium | Mg |
| 13 | Aluminum | Al |
| 14 | Silizium | Si |
| 15 | Phosphor | P |
| 16 | Schwefel | S |
| 17 | Chlor | Cl |
| 18 | Argon | Ar |
| 19 | Kalium | K |
| 20 | Kalzium | Ca |
| 21 | Scandium | Sc |
| 22 | Titan | Ti |
| 23 | Vanadium | V |
| 24 | Chrom | Cr |
| 25 | Mangan | Mn |
| 26 | Eisen | Fe |
| 27 | Kobalt | Co |
| 28 | Nickel | Ni |
| 29 | Kupfer | Cu |
| 30 | Zink | Zn |
| 31 | Gallium | Ga |
| 32 | Germanium | Ge |
| 33 | Arsen | As |
| 34 | Selen | Se |
| 35 | Brom | Br |
| 36 | Krypton | Kr |
| 37 | Rubidium | Rb |
| 38 | Strontium | Sr |
| 39 | Yttrium | Y |
| 40 | Zirkonium | Zr |
| 41 | Nobium | Nb |
| 42 | Molybdän | Mo |
| 43 | Technetium | Tc |
| 44 | Ruthenium | Ru |
| 45 | Rhodium | Rh |
| 46 | Palladium | Pd |
| 47 | Silber | Ag |
| 48 | Kadmium | Cd |
| 49 | Indium | In |
| 50 | Zinn | Sn |
| 51 | Antimon | Sb |
| 52 | Tellur | Te |
| 53 | Jod | I |
| 54 | Xenon | Xe |
| 55 | Cäsium | Cs |
| 56 | Barium | Ba |
| 57 | Lanthan | La |
| 58 | Cer | Ce |
| 59 | Praseodym | Pr |
| 60 | Neodym | Nd |
| 61 | Promethium | Pm |
| 62 | Samarium | Sm |
| 63 | Europium | Eu |
| 64 | Gadolinium | Gd |
| 65 | Terbium | Tb |
| 66 | Dysprosium | Dy |
| 67 | Holmium | Ho |
| 68 | Erbium | Er |
| 69 | Thulium | Tm |
| 70 | Ytterbium | Yb |
| 71 | Lutetium | Lu |
| 72 | Hafnium | Hf |
| 73 | Tantal | Ta |
| 74 | Wolfram | W |
| 75 | Rhenium | Re |
| 76 | Osmium | Os |
| 77 | Iridium | Ir |
| 78 | Platin | Pt |
| 79 | Gold | Au |
| 80 | Quecksilber | Hg |
| 81 | Thallium | Tl |
| 82 | Blei | Pb |
| 83 | Wismut | Bi |
| 84 | Polonium | Po |
| 85 | Astat | At |
| 86 | Radon | Rn |
| 87 | Franzium | Fr |
| 88 | Radium | Ra |
| 89 | Aktinium | Ac |
| 90 | Thorium | Th |
| 91 | Protactinium | Pa |
| 92 | Uran | U |
| 93 | Neptunium | Np |
| 94 | Plutonium | Pu |
| 95 | Amerikium | Am |
| 96 | Curium | Cm |
| 97 | Berkelium | Bk |
| 98 | Kalifornium | Cf |
| 99 | Einsteinium | Es |
| 100 | Fermium | Fm |
| 101 | Mendelevium | Md |
| 102 | Nobelium | No |
| 103 | Lawrencium | Lr |
| 104 | Rutherfordium | Rf |
| 105 | Dubnium | Db |
| 106 | Seaborgium | Sg |
| 107 | Bohrium | Bh |
| 108 | Hassium | Hs |
| 109 | Meitnerium | Mt |
Mit Hilfe dieses Programms lassen sich unter anderem Grafiken für Arbeitsblätter zur nichtkommerziellen Nutzung für Unterrichtszwecke erstellen. Beachten Sie hierbei jedoch, dass jede Art gewerblicher Nutzung dieser Grafiken und Texte untersagt ist und dass Sie zur Verfielfältigung hiermit erstellter Arbeitsblätter und Unterrichtsmaterialien eine schriftliche Genehmigung des Autors (unseres Unternehmens) benötigen.
Diese kann von einem registrierten Kunden, der im Besitz einer gültigen Softwarelizenz für das entsprechende Programm ist, bei Bedarf unter der ausdrücklichen Schilderung des beabsichtigten Verfielfältigungszwecks sowie der Angabe der Anzahl zu verfielfältigender Exemplare für das entsprechende Arbeitsblatt unter der auf der Impressum-Seite dieses Angebots angegebenen Email-Adresse eingeholt werden. Es gelten unsere AGB.
Dieses Programm eignet sich neben seinem Einsatz als Berechnungs- bzw. Animationsprogramm zudem zum Lernen, zur Aneignung entsprechenden Fachwissens, zum Verstehen sowie zum Lösen verschiedener Aufgaben zum behandelten Fachthema. Durch seine einfache interaktive Handhabbarkeit bietet es die auch Möglichkeit der Durchführung unterschiedlicher Untersuchungen hierzu. Des Weiteren eignet es sich beim Üben dazu, um das Erlernte hinsichtlich praktizierter Übungen bzw. bearbeiteter Übungsaufgaben zu überprüfen und hierzu erworbenes Wissen festigen zu können.
Es kann sowohl zur Einführung in das entsprechende Fachthemengebiet, wie auch zur Erweiterung des bereits hierzu erlangten Fachwissens sowie als Unterstützung bei der Bearbeitung von Anwendungsaufgaben genutzt werden. Des Weiteren eignet es sich auch als Begleiter bei der Bearbeitung von Abituraufgaben sowie zur Vorbereitung auf Klassenarbeiten, zur Unterstützung bei der Abiturvorbereitung und zur Intensivierung des erforderlichen Wissens beim Abitur (Abi) im entsprechenden Leistungskurs (LK).
Mittels der anschaulichen Gestaltung und einfachen Bedienbarbarkeit einzelner Module dieser Software können Fragen zum entsprechenden Themengebiet, die mit den Worten Was ist?, Was sind?, Wie?, Wieviel?, Was bedeutet?, Weshalb?, Warum? beginnen beantwortet werden. Dieses Programm kann auch dabei behilflich sein, einen Begriff zum entsprechenden Fachthema zu erklären.
Bei Fragen deren Wörter Welche?, Welcher?, Welches?, Wodurch? bzw. Wie rechnet man? oder Wie berechnet man? sind, können zugrunde liegende Sachverhalte oftmals einfach erklärt und nachvollzogen werden. Auch liefert diese Applikation zu vielen fachthemenbezogenen Problemen eine Antwort und stellt eine diesbezüglich verständliche Beschreibung bzw. Erklärung bereit.
Eine kleine Übersicht in Form von Bildern und kurzen Beschreibungen über einige zu den einzelnen Fachthemengebieten dieses Programms implementierte Unterprogramme finden Sie unter Kurzbeschreibungen von Modulen zum Themengebiet Mechanik - Kurzbeschreibungen von Modulen zum Themengebiet Elektrotechnik - Kurzbeschreibungen von Modulen zum Themengebiet Optik - Kurzinfos zum Themengebiet Thermodynamik sowie unter Kurzbeschreibungen von Modulen zu sonstigen Themengebieten.
Hilfreiche Informationen zu diesem Fachthema sind unter Wikipedia - Bohrsches Atommodell zu finden.
Nachfolgend finden Sie ein Video zu diesem Fachthema, welches Sie durch die Ausführung eines Klicks
auf die nachfolgend gezeigte Grafik abspielen lassen können.
Schräger Wurf - Schiefer Wurf, Waagerechter Wurf - Horizontaler Wurf, Hookesches Gesetz, Mechanische Arbeit, Zweites Newtonsches Gesetz, Drittes Newtonsches Gesetz, Gedämpfte mechanische Schwingung, Bewegungen auf einer Kreisbahn, Hebelgesetz, Chaotisches Doppelpendel, Mathematisches Pendel, Freier Fall und Luftwiderstand, Harmonische Schwingungen, Molekularbewegungen, Brownsche Bewegungen, Potentielle und kinetische Energie, Ideale Strömung - Volumenstrom, Druck in Flüssigkeiten, Wellen - Simulationen, Zusammengesetzte Bewegung, Bewegungen in der Ebene, Carnotscher Kreisprozess, Adiabatische Zustandsänderung, Isotherme Zustandsänderung, Isobare Zustandsänderung, Isochore Zustandsänderung, Beugung am Spalt, Hohlspiegel, Sammellinse, Zerstreuungslinse, Wechselstromkreise, RLC-Kreis - RLC-Schaltung, RL-Kreis - RL-Schaltung, RC-Kreis - RC-Schaltung, Resonanz - Resonanzkurve, Widerstände im Wechselstromkreis, Schwingungen und deren Überlagerung, Plattenkondensator, Ladung und Entladung von Kondensatoren, Reihenschaltung und Parallelschaltung, Lissajou-Figuren, 1. Keplersches Gesetz, 2. Keplersches Gesetz, 3. Keplersches Gesetz
Formelbibliothek - Raumgittermodelle - Schalenbelegung-Orbitalbelegung - Keplersche Gesetze - Kalender
Unterprogramm Bohrsches Atommodell
PhysProf 1.1 - Unterprogramm RLC-Kreis
MathProf 5.0 - Unterprogramm Kurven in Parameterform

SimPlot 1.0 - Grafik- und Animationsprogramm für unterschiedlichste Anwendungszwecke
Nachfolgend finden Sie ein Video zu einem in PhysProf 1.1 unter dem Themenbereich Mechanik eingebundenen Unterprogramm,welches Sie durch die Ausführung eines Klicks auf die nachfolgend gezeigte Grafik abspielen lassen können.
Nachfolgend finden Sie ein Video zu einem in PhysProf 1.1 unter dem Themenbereich Elektrotechnik eingebundenen Unterprogramm, welches Sie durch die Ausführung eines Klicks auf die nachfolgend gezeigte Grafik abspielen lassen können.
Nachfolgend finden Sie ein Video zu einem in PhysProf 1.1 unter dem Themenbereich Thermodynamik eingebundenen Unterprogramm, welches Sie durch die Ausführung eines Klicks auf die nachfolgend gezeigte Grafik abspielen lassen können.
Nachfolgend finden Sie ein Video zu einer mit SimPlot 1.0 erstellten Animationsgrafik, welches Sie durch die Ausführung eines Klicks auf die nachfolgend gezeigte Grafik abspielen lassen können.
Nachfolgend finden Sie ein Video zu einer mit SimPlot 1.0 erstellten Animationsgrafik, welches Sie durch die Ausführung eines Klicks auf die nachfolgend gezeigte Grafik abspielen lassen können.
Nachfolgend finden Sie ein Video zu einer mit SimPlot 1.0 erstellten Animationsgrafik, welches Sie durch die Ausführung eines Klicks auf die nachfolgend gezeigte Grafik abspielen lassen können.